Oxidare si reducere
Reactia de combinare cu oxigenul este o reactie de
oxidare. Sa analizam reactia de oxidare a magneziului:
![]()
Atomul de magneziu cedeaza
doi electroni atomului de oxigen, trecand in ion magneziu, Mg2+.
![]()
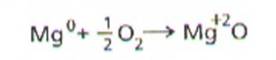 Magneziul
isi mareste numarul de oxidare de la 0, in magneziul metalic, la +2 in oxidul
de magneziu.
Magneziul
isi mareste numarul de oxidare de la 0, in magneziul metalic, la +2 in oxidul
de magneziu.
Reactia in care se scoate oxigenul dintr-o
combinatie este o reactie de reducere. Sa analizam reactia de reducere, cu
hidrogen, a oxidului de cupru.
![]()
In aceasta reactie, ionul
de cupru, Cu2+, accepta doi electroni si trece in atomul de cupru.
![]()
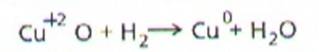 Cuprul
isi micsoreaza numarul de oxidare de la
+2, in oxidul de cupru, la 0 in cuprul metalic.
Cuprul
isi micsoreaza numarul de oxidare de la
+2, in oxidul de cupru, la 0 in cuprul metalic.
Pornind de la aceste
observatii, s-au generalizat notiunile de oxidare si reducere si au fost
definite astfel:
Procesul de oxidare este transformarea ce are loc cu cedare de
electroni. In procesul de oxidare, numarul de oxidare creste.
Procesul de reducere este transformarea ce are loc cu
acceptare de electroni. In procesul de reducere, numarul de oxidare scade.
Conform
acestei noi acceptiuni, nu numai reactiile de combinare cu oxigenul sunt
reactii de oxidare. Orice proces ce are loc cu cedare de elctron si cu marirea
numarului de oxidare este un proces de oxidare.
Astfel, in reactiile:
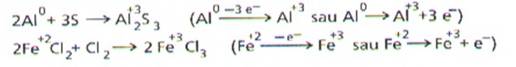
atomii de aluminiu si, respectiv, ionii Fe2+ participa la
procese de oxidare.
In aceeasi acceptiune, nu numai reactiile ce au loc cu micsorarea
continutului in oxigen sunt reactii de reducere. Orice proces ce are loc cu
acceptare de electroni si cu miscarea numarului de oxidare este un proces de
reducere.
Astfel, in reactiile:
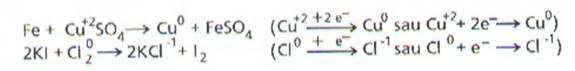
ionii de cupru, Cu2+, si respectiv atomii de
clor participa la
procese de reducere.
Procesele de reducere si
de oxidare nu pot fi separate. Electronii cedati de un atom sunt acceptati de
un alt atom. De aceea, un proces de
oxidare este intotdeauna cuplat cu un
proces de reducere intr-o reactie de oxido-reducere sau reactie redox.
Astfel, in reactia:
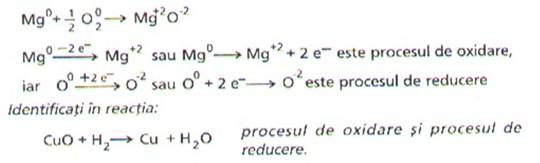
Specia chimica (atom, ion) care cedeaza electronii acceptati
in procesul de reducere, deci favorizeaza reactia de reducere, se numeste agent
reducator. Agentul reducator se oxideaza.
In
reactia de combinare a magneziului cu oxigenul, magneziul este agentul
reducator. Atomul de magneziu cedeaza electronii care sunt acceptati de atomul
de oxigen in procesul de reducere.
Specia chimica (atom, ion) care accepta electronii cedati in procesul
de oxidare, deci favorizeaza reactia de oxidare, se numeste agent oxidant.
Agentul oxidant se reduce.
In
reactia de ardere a magneziului, oxigenul este agentul oxidant. Atomul de
oxigen accepta electronii cedati de atomul de magneziu in procesul de oxidare.
![]() Procesele
de cedare si de acceptare de electroni pot fi reale sau formale. Astfel, in
reactia:
Procesele
de cedare si de acceptare de electroni pot fi reale sau formale. Astfel, in
reactia:
are loc un transfer real de electroni de la atomii de magneziu, care se
oxideaza trecand in ionii Mg2+ , la atomii de oxigen, care se reduc
la ionii de O2-. ![]()